Синдром патау
Содержание:
- 2.Причины
- НАШИ ПАРТНЕРЫ
- Перемена места
- Причины генных нарушений
- Лечение
- Существуют ли факторы риска? Что может спровоцировать появление мутации?
- Лечение заячьей губы
- Типы наследственных заболеваний
- Какова точность теста НИПТ?
- Описание
- Лечение заячьей губы
- Этиология и эпидемиология
- Следует ли через некоторое время повторить пренатальный генетический тест?
- Диагностика
2.Причины
Как указано в нозологической формулировке, наследственная ладонная и подошвенная эритема является генетической аномалией; в ее основе лежит неправильное формирование сети венозно-артериальных анастомозов (сообщений) в кровеносной системе кистей и ступней. Следствием оказывается нарушения микроциркуляции и повышение давление в артериолах и капиллярах дистальных отделов конечностей, что и проявляется красным оттенком кожи.
В некоторых случаях эритроз Лане отсутствует при рождении и манифестирует уже в зрелом или даже пожилом возрасте под влиянием определенных триггерных факторов (чаще всего это интоксикация или гормональный дисбаланс вследствие дисфункции половых желез).
Следует отметить, что в одних источниках к пусковым факторам наследственной ладонной и подошвенной эритемы относятся также иммуноаллергические механизмы, тогда как другие авторы аллергические эритрозы из понятия болезнь Лане исключают.
НАШИ ПАРТНЕРЫ
Перемена места
На первый взгляд перемена мест в хромосомах их участков не должна вызывать патологий – какая разница, где стоит код того или иного белка? Ан нет, разница огромная, то, как проявит себя ген, очень сильно зависит от соседствующих кодов. Особенно сильно проявляются транслокации в негомологичных хромосомах, то есть когда фрагмент хромосомы из одной пары переносится в пару с другими номером.
На сегодняшний день установлена причина хронического миелолейкоза – это также нарушения в хромосомах. Так называемая «филадельфийская хромосома» представлена транслокацией части 22-й хромосомы на часть 9-й.
Причины генных нарушений
О возможных причинах роста числа генетических заболеваний и методах психосоциальной реабилитации я беседую с Гуткевич Еленой Владимировной, врачом-генетиком, доктором медицинских наук, ведущим научным сотрудником НИИ психического здоровья г. Томска, профессором кафедры генетической и клинической психологии факультета психологии НИ ТГУ.
– Елена Владимировна, каковы возможные причины увеличения числа генетических заболеваний?
– Частота их увеличивается, прежде всего, за счет значительно выросшей диагностики, существенное развитие методов генетики, в том числе молекулярной. Однако сложность и недостаточная разработанность этой проблемы требуют вклада генетических, конституционально-биологических и средовых факторов риска в возникновение. Необходимо исследовать клинический полиморфизм наиболее распространенных нервно-психических расстройств у взрослых, детей и подростков (пограничные нервно-психические расстройства, шизофренические расстройства, умственная отсталость), что позволит решать вопросы современных мер превенции, психосоциальной реабилитации. При исследовании многофакторных заболеваний, многих соматических и психических расстройств (РДА, ДЦП, УО, ЗПР), пока не удается обнаружить один ген или хромосомную патологию, которые могут быть причиной их появления. Важнейшее значение имеют внешние факторы – семейные, средовые (психологические в том числе). Хромосомные мутации происходят под влиянием значительных сдвигов в экологической системе и изменении состава многих продуктов питания (ГМО).
Ученые института генетики г. Томска сравнивали количество легко диагностируемых врожденных пороков с некоторыми российскими и зарубежными данными. Частота врожденных пороков в Томске составила 12,4 на 1000 новорожденных; в Москве – 17,2; по Курской области – 14,19; в Клину – 10,5; по Тульской области – 14,6. А в двадцати европейских странах частота врожденных пороков находится в диапазоне от 8,7 до 21,2. Из-за изменения радиационного фона за последние 20 лет чаще стали рождаться дети с пороками сердечно-сосудистой системы, половых органов, костно-мышечной системы, с пороками лица и шеи, мочевой системы, с атрезией пищевода, агенезией и дисгенезией почек.
Лечение
Вылечить синдром Патау невозможно. Патология приводит к возникновению нарушений в развитии и строении внутренних органов. Медики могут попытаться облегчить состояние ребенка. Для этого проводится оперативное вмешательство. Чаще всего при синдроме Патау выполняется:
- Пластика лица. У многих пациентов при этом недуге наблюдаются расщелины на губах. Врачи устраняют этот недостаток.
- Удаление дополнительной матки. Аналогичное действие выполняется в отношении других подобных патологий, если они имеют место быть.
- Проводятся операции на внутренних органах. Обычно лечение осуществляется в отношении почек, мочеточников и сердца. Это позволяет облегчить уход за ребёнком.
Дополнительно проводится симптоматическое лечение. Врачи устраняют сопутствующие симптомы и укрепляют иммунитет ребенка. Действия необходимо выполнять для того, чтобы избежать воспаления органов. Дети с синдромом Патау всегда недоразвитые. Это касается физического и умственного развития. Полноценной жизнью жить такие пациенты вряд ли могут. Ребёнок не будет самостоятельным. Именно поэтому врачи рекомендуют прервать беременность на сроке до 22 недель.
Существуют ли факторы риска? Что может спровоцировать появление мутации?
Синдром Патау развивается спонтанно и предупредить его, увы, невозможно. Тем не менее учеными выделено несколько неблагоприятных факторов.
- Считается, что риск появления подобной патологии повышается в том случае, если мать проживает в районе с плохой экологической ситуацией.
- Как уже упоминалось, определенную роль в появлении спонтанных хромосомных мутаций играет радиационное облучение.
- Замечено также, что вероятность появления различных хромосомных и генетических мутаций увеличивается в случае поздней беременности (мать старше 45 лет).
- К факторам риска относят наличие наследственных заболеваний в предыдущих поколениях родителей.
- Доказано, что случаи генетических и хромосомных мутаций учащаются если речь идет о браках между близкими родственниками.
Лечение заячьей губы
Устранение такого дефекта, как заячья губа, проводится с помощью пластической хирургии.
Выделяют следующие типы оперативного хирургического вмешательства, применяемые для лечения заячьей губы:
- хейлопластика;
- ринохейлопластика;
- ринохейлогнатопластика.
Если доношенный новорожденный не имеет иных пороков развития, а также противопоказаний к операции, возможно проведение реконструктивной пластической операции уже в течение первого месяца жизни, но обычно детей, страдающих заячьей губой, оперируют в возрасте от 3 до 6 месяцев.
Хейлопластика
Хейлопластика
Современная хейлопластика располагает разнообразными методиками, которые направлены на устранение эстетической и функциональной неполноценности пациента с заячьей губой.
Хейлопластика – это пластическая операция по коррекцию верхней губы. Подобное вмешательство требует предварительного обширного медицинского обследования пациента.
В процессе хейлопластики хирург выполняет сопоставление фрагментов тканей и их соединение. Для максимальной защиты швов в носовую полость необходимо на некоторое время ввести марлевый тампон, который затем извлекается. На его место устанавливается специальная трубка сроком до 90 суток после окончания вмешательства.
Швы после операции снимаются через 10 суток с момента проведения операции по устранению заячьей губы. Иногда после хейлопластики требуется дополнительно медицинское сопровождение для полного удаления любых остаточных явлений данного нарушения.
Ринохейлопластика
Ринохейлопластика – пластическая операция, подразумевающая большую сложность, чем хейлопластика. Подобное вмешательство представляет собой одновременные лечебные хирургические манипуляции, которые направлены не только на устранение заячьей губы, но и на коррекцию носовых хрящей и мышечной части ротовой полости.
Ринохейлогнатопластика
Ринохейлогнатопластика – это особая костная пластическая операция незаращения альвеолярного отростка, являющаяся наиболее сложным вмешательством среди трех возможных вариантов устранения заячьей губы. Она применяется в таких случаях, когда нарушения скелета лица отличаются высокой степенью тяжести.
Операция помогает устранить недоразвитие и деформацию передней части верхней челюсти, она способна улучшить форму верхней губы и уменьшить дефект носовых хрящей, связанный с ней, а также снижает до минимума вероятность развития отклонений челюстно-зубного развития.
Помимо прочего, ринохейлогнатопластика отвечает за формирование мышечного каркаса полости рта в норме. Проведение подобной операции является типичной хирургической практикой для детей, страдающих от расщелины неба или губы.
Эффективность лечения
Заячья губа после операции обычно устраняется полностью в 85-90% случаев. Это гарантирует в будущем нормальную адаптацию растущего человека в социальной среде. Результаты проведенной операции (как функциональные, так и эстетические) оцениваются спустя 12 месяцев со дня ее проведения.
Заячья губа после операции обычно устраняется полностью в 85-90% случаев. Это гарантирует в будущем нормальную адаптацию растущего человека в социальной среде. Результаты проведенной операции (как функциональные, так и эстетические) оцениваются спустя 12 месяцев со дня ее проведения.
Профилактика нарушения
Для профилактики появления патологии будущей маме необходимо:
-
отказаться от вредных привычек;
-
обследоваться на наличие ИППП;
-
избегать стрессов;
-
если в семье есть любое генетическое заболевание, необходимо проконсультироваться с врачом-генетиком.
Отопластика – пластическая операция, занимающая одну из лидирующих позиций на рынке спроса услуг пластической хирургии. Она проводится по разным показаниям и …
Читать далее >>
Типы наследственных заболеваний
Наследственные заболевания делятся на три типа: моногенные, полигенные (или многофакторные) и хромосомные. В основе моногенных заболеваний лежит мутация одного гена, которая локализована в одной хромосоме и провоцирует обменные процессы в организме.
Моногенные и полигенные генетические болезни
К моногенным наследственным заболеваниям относятся: синдром Марфана, хорея Гентингтона, муковисцидоз, фенилкетонурия, миопатия Дюшена, гемофилия и др. При полигенных (многофакторных) болезнях с наследственной предрасположенностью соотношение больных не соответствует теории расщепления, которую придумал основоположник генетики Г.И. Мендель. Для патологического проявления мутантного гена обязательно действие специфического внешнего фактора, например лекарственных препаратов (тератогенное действие), химических веществ или биологических агентов. Без воздействия специфического фактора даже при наличии в генотипе мутантного гена заболевание не развивается. Полигенные болезни обусловлены взаимодействием нескольких генов с факторами окружающей среды. К полигенным наследственным болезням относятся гипертоническая болезнь, атеросклероз, язвенная болезнь желудка и двенадцатиперстной кишки, сахарный диабет обоих типов, аллергические заболевания, гепатит, ревматоидный артрит, лейкоз, ишемическая болезнь сердца, онкологические заболевания, психические расстройства и др.
Хромосомные болезни
К хромосомным относят болезни, связанные с геномными мутациями или структурными изменениями отдельных хромосом. Возникают они в результате мутаций в половых клетках одного из родителей. Из поколения в поколение передаются не более 3-5% из них. Хромосомные нарушения приводят к 50% спонтанных абортов, и 7% всех мертворождений. Хромосомные болезни возникают как из-за изменения количества и структуры хромосом, так и нерасхождением хромосом на ранней стадии дробления зиготы, которые приводят к развитию мозаицизма, а также из-за ломкости Х-хромосомы.
Из числа количественных нарушений хромосом общеизвестны такие болезни, как болезнь Дауна (трисомия по 21-й хромосоме), синдром Эдвардса (трисомия по 18-й хромосоме), синдром Патау (трисомия по 13-й хромосоме), синдром Шерешевского-Тернера (отсутствие одной Х хромосомы у женщин), синдром Клайнфельтера (лишняя Х-хромосома у мужчин), синдром дисомии по У-хромосоме у мужчин.
К внутрихромосомным мутациям относятся болезни: синдром-Прадера-Вилли (отсутствие 7-ми генов из 15-й хромосомы), синдром Ангельмана (критичность региона 15-й хромосомы материнского происхождения). Структурные нарушения хромосом приводят к таким болезням, как синдром «Кошачьего крика» (утрата короткого плеча 5-й хромосомы), а ломкость Х-хромосомы к одноименной болезни (синдром Мартина-Белла). Примерно у 30-40% больных с синдромом ломкой Х-хромосомы клиническая картина имеет выраженный шизофреноподобный характер, в первую очередь это аутистические признаки и двигательные расстройства кататоноподобного характера.
Отдельно хочется сказать о дисомии по У-хромосоме, поскольку это заболевание, вызванное добавочной У-хромосомой у мужчин, может привести к опасным последствиям. Признаками кариотипа 47 ХУУ являются высокий рост (186-200 см), акромегалия, непропорциональное увеличение дистальных отделов конечностей, физическая сила, интеллект не ниже среднего. Лишняя У-хромосома определяет эмоционально-волевые нарушения, приводит к агрессии, многие обладают способностью давить на психику взглядом. Если произойдет сбой, то возможны однотипные, серийные преступления. За всю историю криминалистики среди серийных убийц с помощью скрининга был выявлен лишь один человек с лишней У-хромосомой. Если обследование подтверждает у убийцы наличие лишней У-хромосомы, то его отправляют не за решетку, а в клинику. Из мирового кинематографа известен такой представитель кариотипа 47 ХУУ, как Доктор Ганнибал Лектер из «Молчания ягнят».
Какова точность теста НИПТ?
НИПТ является высокоточным методом. Его точность по результатам многочисленных исследований составляет до 99,9%. При этом отмечен низкий процент необходимости перезабора крови в связи с недостатком плодовой ДНК в образце (менее 3% случаев), низкий процент ложно положительных результатов (то есть тех случаев, когда при положительном результате теста ребенок оказывается здоров — не более 0,72% или 1 случая на 140). Это означает, что лишь в 1 случае из 140 положительных результатов теста патология плода не будет подтверждена, а в 139 случаях — тест позволит ее выявить.
Частота ложноотрицательных результатов (то есть случаев, когда тест будет отрицательным при имеющейся патологии плода) составляет не более 1 случая на 10 000 тестов.
Тем не менее, принимая решение о проведении теста, нужно полностью отдавать себе отчет в том, что данный тест не является диагнозом, а лишь с очень высокой вероятностью позволяет заподозрить хромосомную патологию плода. В случае если будет заподозрена серьезная патология плода и будет обсуждаться вопрос о возможности/ невозможности сохранения беременности — потребуется подтверждение с помощью дополнительных тестов — биопсии ворсин хориона, амниоцентеза и пр., т.е. инвазивной диагностики. Однако, в связи с крайне низким процентом ложноположительных результатов такие исследования потребуются на порядок реже, чем при проведении стандартного скрининга.
Описание
Резус-фактор (Rh) — это антиген (белок), который находится на поверхности эритроцитов, причём наиболее иммуногенным является антиген D (RhD), присутствие которого и определяет положительный резус-фактор (Rh+). Исследование выполняется с 9 полных недель беременности, т. е. с 10 недели.Для проведения исследования необходимо предоставить копию УЗИ.
Если резус-отрицательная (Rh-) женщина беременна резус-положительным (Rh+) плодом, её иммунная система начинает вырабатывать анти-D-антитела, вызывающие разрушение эритроцитов плода. Как правило, анти-D-антитела отсутствуют при первой беременности Rh+ плодом, протекающей без осложнений, однако сенсибилизация матери возникает в процессе родов. При каждой последующей беременности или при повреждении плаценты увеличивается риск развития гемолитической болезни плода. 98% случаев гемолитической болезни новорождённых связаны именно с D-резус-антигеном. При раннем проявлении резус-конфликт может стать причиной нарушения развития плода, преждевременных родов или выкидышей.Ген RHD
Делеция гена RHD в обеих гомологичных хромосомах обуславливает отрицательный резус-фактор. Наличие гена в гомозиготном или гетерозиготном состоянии определяет положительный резус-фактор у обследуемого. В случае если резус-положительные отцы являются гетерозиготными по резус-фактору, то у резус-отрицательных матерей даже при наличии отягощённого анамнеза плод в 50% случаев будет резус-отрицательным. Таким образом, для женщин с резус-конфликтной беременностью появилась возможность проведения пренатальной диагностики с целью определения резус-фактора на ДНК плода, выделенной из ворсин хориона (10–15 недель беременности) или из амниотической жидкости при проведении амниоцентеза (24 неделя беременности).
Если результаты молекулярно-генетического анализа показывают, что плод является резус-отрицательным, то отпадает необходимость в проведении последующих инвазивных процедур, и такие пациентки исключаются из дальнейшего обследования по тяжести развития гемолитической болезни плода. Кроме того, определение гетерозиготного генотипа по резус-фактору (RHD+/RHD-) у отца даёт основание для проведения преимплантационной диагностики при наличии отягощённого акушерского анамнеза (гибель детей от гемолитической болезни) и резус-сенсибилизации у матери. В результате при ЭКО будущей матери будут перенесены только резус-отрицательные эмбрионы.
Так как антирезусную профилактику иммуноглобулином человека рекомендовано проводить на 28 неделе первой и последующих беременностей, то определение резус-фактора плода на ранних сроках является необходимым. Определение Rh- плода в 1–2 триместре беременности позволит сократить расходы на регулярное определение титра анти-D-антител и антирезусную профилактику.Показания
Беременным (Rh-)-женщинам с 12 по 27 неделю беременности, если (Rh+)-отец является гетерозиготным носителем гена RhD (Генотипирование системы RhD).Подготовка
Специальная подготовка не требуется. Рекомендуется взятие крови не ранее чем через 4 часа после последнего приема пищи.Интерпретация результатов
При отрицательном результате теста, статус плода считается с высокой вероятностью резус-отрицательным, однако рекомендуется повторять тест на более поздних сроках беременности (но не позднее 27-ой недели) для подтверждения.
Положительный результат теста считается показанием к введению антирезусного иммуноглобулина, однако вопрос о его введении должен решаться только акушером-гинекологом на основании и других методов диагностики резус-конфликта.
При отсутствии антител к Rh-фактору по результатам ИФА и положительном молекулярно-генетическом тесте, рекомендуется введение антирезусного иммуноглобулина в период от 28 недель беременности (для профилактики ГБН) и не позднее 72 часов после родов (для профилактики Rh-конфликта при следующей беременности).
Лечение заячьей губы
Исправляют дефект только оперативным путем. Хейлопластика проходит поэтапно. Число операций, объем и сроки определяет врач. Следует обратиться к оториноларингологу, логопеду, психологу, фониатру, стоматологу-ортодонту и сурдологу, поскольку заячья губа провоцирует понижение иммунитета, ухудшение слуха и речи. Перед хирургическими действиями обязательна серьезная забота о ротовой полости, чтобы исключить появление кариеса и других заболеваний. В послеоперационное время необходимо следить, чтобы в раны не попала инфекция.
Операция по поводу заячьей губы
Заячья губа исправляется оперативным путем. Операция включает в себя несколько этапов
Сначала важно не только устранить косметический дефект, но и восстановить анатомию. Малышу осуществляют пластику носа и губ
Пластика неба делается до достижения ребенком полутора лет. Применяют общий наркоз. Снять швы можно через неделю. Пластика неба предполагает пребывание в стационаре в течении пяти дней. Финальная операция, пластика верхней челюсти, планируется с восьми до двенадцати лет, когда у ребенка появляются постоянные зубы.
Пластика заячьей губы
Заячья губа подлежит пластике. Первичная хейлопластика проводится в первые дни жизни младенца. Так восстанавливают полноценность расщепленной до этого губы. В раннем возрасте выполняются разные методы хейлопластики. Выбор методики осуществляет врач, руководствуясь формой дефекта.
Если необходимо откорректировать губу, нос и мышцы области рта, выполняют первичную ринохейлопластику. Такое вмешательство считают сложным.
Восстановление полноценности губ и носа и устранение дефектов отростка альвеолы решается путем выполнения ринохейлогнатопластики.
Всестороннее обследование пациента предшествует хейлопластике. Медикам необходимо получить подтверждение, что ребенок готов к хирургическому вмешательству.
После завершения пластики заячьей губы устанавливают марлевый тампон в носу, чтобы защитить швы. Затем тампон на 3 месяца заменяют трубочкой из пластмассы, чтобы исключить деформацию носа. Через неделю после операции снимают швы.
Послеоперационный рубец виден, но в дальнейшем его можно уменьшить, обратившись к косметологическим процедурам.
Этиология и эпидемиология
Встречается с частотой 1:7000-1:14000. Имеются два цитогенетических варианта синдрома Патау: простая трисомия и робертсоновская транслокация. Другие цитогенетические варианты (мозаицизм, изохромосома, неробертсоновские транслокации) обнаружены, но они встречаются крайне редко. Клиническая и патологоанатомическая картины простых трисомных форм и транслокационных не различается. 75 % случаев трисомии хромосомы 13 обусловлено появлением дополнительной хромосомы 13. Между частотой возникновения синдрома Патау и возрастом матери прослеживается зависимость, хотя и менее строгая, чем в случае синдрома Дауна. 25 % случаев СП — следствие транслокации с вовлечением хромосом 13-й пары, в том числе в трёх из четырёх таких случаев мутация de novo. В четверти случаев транслокация с вовлечением хромосом 13-й пары имеет наследственный характер с возвратным риском 14 %.
Соотношение полов при синдроме Патау близко к 1:1. Дети с синдромом Патау рождаются с истинной пренатальной гипоплазией (на 25 — 30 % ниже средних величин), которую нельзя объяснить небольшой недоношенностью (средний срок беременности 38,5 недель).
Следует ли через некоторое время повторить пренатальный генетический тест?
Нет необходимости повторять генетический пренатальный тест позже, во время той же беременности. Если результат неинвазивного теста вызывает тревогу, то только тогда он должен быть подтвержден такими тестами, как амиоцентез или взятие проб ворсинок хориона.
Неинвазивное пренатальное тестирование не представляет опасности ни для плода, ни для матери.
Инвазивное пренатальное тестирование – вторая группа диагностических процедур, которые выполняются гораздо реже – в тех случаях, когда есть четкие показания. Это ограничение связано с тем фактом, что инвазивное тестирование может быть неудобным для матери и представляет небольшой риск выкидыша или внутриутробной инфекции.
Среди инвазивных тестов наиболее распространенным типом является амниоцентез – тест, который включает пункцию плодного пузыря и сбор околоплодных вод, содержащих клетки плода.
Амниоцентез – тест
Диагностика
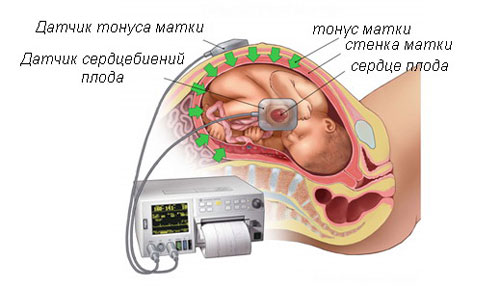
Все хромосомные болезни диагностируются по одному принципу. На первом этапе скрининга проводится УЗИ и определение биохимических маркеров (РАРР-А, бета-ХГЧ). Данные дают во время пренатальной диагностики возможность определить степень риска рождения ребенка с хромосомной аномалией. Дальнейшая инвазивная диагностика синдрома Патау с постановкой цитогенетического диагноза при высокой вероятности заболевания проводится следующим образом:
- на 8-12 неделе беременности – биопсия ворсин хориона;
- на 14-18 неделе беременности – амниоцентез;
- после 20 недели беременности – кордоцентез.
Полученный в результате исследований материал изучается по методу КФ-ПЦР или кариотипированием с дифференциальной окраской. Выявляется 13 хромосома и по результатам УЗИ, врач ориентируется на клинические признаки не матери, а ребенка. Подтвердить болезнь Патау можно только с помощью дородовой диагностики, которая отвечает за определение хромосомного набора младенца. При высокой вероятности наследственного заболевания младенцу проводят тщательнейшее обследование, которое включает:
- нейросонографию;
- УЗИ почек, брюшной полости;
- эхокардиографию и прочее.