Лечение адреногенитального синдрома
Содержание:
- Зачем нужен в организме?
- 1.Общие сведения
- Как развивается заболевание
- Online-консультации врачей
- 1.Общие сведения
- Причины адреногенитального синдрома
- Почему необходимо обратиться в клинику «Мама Папа Я»
- Симптомы дисфункции коры надпочечников
- Виды урогенитальных расстройств
- Описание
- Расстройство уродинамики
- К каким докторам следует обращаться если у Вас Дисфункция коры надпочечников (адреногенитальный синдром) и беременность:
- Методы диагностики адреногенитального синдрома
- 3.Симптомы и диагностика
- Механизм наследования генитального синдрома
- Патогенез (что происходит?) во время Адреногенитального синдрома:
Зачем нужен в организме?
Соединение F вырабатывается корой надпочечников, стимулирует углеводный и белковый обмен. Это необходимо для восстановления клеток и тканей организма, его стабильной работы, нутриентов. Помогает бороться с вирусами и бактериями. Низкий уровень негативно сказывается на иммунной системе и работе организма в целом.
Поэтому полезно узнать, зачем нужен гормон кортизол, за что отвечает в организме:
- за регуляцию кровяного давления;
- обмен глюкозы, сахара и инсулина;
- снимает отечность;
- оказывает антиаллергическое, цитостатическое, противошоковое действие;
- ускоряет вывод токсинов;
- защищает организм от негативного воздействия стресса;
- оказывает непродолжительное противовоспалительное действие.
Снижение уровня кортизола в крови может иметь неприятные симптомы, которые проявляются в резком снижении веса, хронической усталости, недосыпании, болью в районе живота. Самым негативным последствием низкого уровня кортизола в сочетании с сильным стрессом может стать адреналовый криз. Такое состояние требует немедленной госпитализации и оказания квалифицированной помощи.
Повышение может сопровождать обратные процессы:
- ожирение;
- истончение кожи;
- появление растяжек;
- повышение артериального давления.
Любые долговременные отклонения от нормы в выработке гидрокортизона негативно сказываются на организме и самочувствии в целом, поэтому при появлении симптомов необходимо обратиться к врачу. Концентрация поможет врачу выявить целый ряд патологических изменений в организме, которые на ранних стадиях хорошо отвечают на терапевтические процедуры.
1.Общие сведения
Как и большинство эндокринных желез, надпочечники продуцируют несколько гормонов, каждый из которых участвует в регуляции множества взаимосвязанных процессов. Так, в мозговом веществе вырабатываются адреналин, норадреналин, соматостатин и другие биоактивные вещества; кора надпочечников продуцирует глюкокортикоиды, альдостерон, андрогены (половые гормоны – тестостерон, андростерон и т.д.).
Любая диспропорция в естественной гормональной формуле крови, т.е. недостаточная концентрация одних гормонов и аномально высокая концентрация других, приводит к «цепной реакции» эндокринных нарушений и очень серьезным последствиям в функционировании всех систем организма. Особую группу эндокринных расстройств составляют врожденные, чаще всего наследственные тяжелые заболевания, при которых гормональный дисбаланс возникает еще на этапе внутриутробного развития и обнаруживается с момента рождения.
Адреногенитальный синдром принадлежит именно к таким наследственным заболеваниям.
Собирательный диагноз «врождённая гиперплазия коры надпочечников» включает несколько наследственных болезней, обусловленных неправильным кодированием ферментов, необходимых для секреции кортизола и альдостерона (недостаточное содержание 21-гидроксилазы). Адреногенитальный синдром развивается вследствие дефицита кортизола и повышенной продукции адренокортикотропного гормона (АКТГ), «отвечающего» за рост и функционирование коры надпочечников.
Гиперплазия (аномальное увеличение) и гиперпродукция кортикостероидов приводит к избытку андрогенов, – мужских половых гормонов, – или гиперандрогении. Синонимическое название адреногенитального синдрома – вирилизирующая гиперплазия надпочечниковых желез; «вирилизация» означает приобретение организмом утрированных мужских черт (иногда термин употребляется в более широком смысле: приобретение внешних черт и признаков, характерных для противоположного пола).
Распространенность адреногенитального синдрома находится в тесной зависимости от расового и национального состава обследуемых выборок. Среди европеоидов частота встречаемости составляет примерно 1:14 000, тогда как в некоторых семитских популяциях этот показатель достигает 17-19%, а у аборигенов Аляски – 1:286 в выборках новорожденных.
Как развивается заболевание
Синдром Ретта у детей – довольно коварное заболевание. При рождении оно практически не проявляет себя. Первые его симптомы появляются в период от 6 мес. до полутора лет. Однако некоторые, еле заметные признаки, в первом полугодии все-таки имеются. Но они настолько ничтожны, что не привлекают внимания.
Вот что говорит мама одной из девочек с синдромом по поводу первого полугодия ее жизни. Она придала значение этим мелочам только по прошествии 1 года и 7 месяцев с рождения ее дочери, когда проявления стали уже явными. Из предвестников болезни она отметила, что ее малышка начала держать голову в 3 месяца, а не в 2, как это положено. В 6 месяцев она еще не могла сидеть, а ходить начала только в 1 год и 4 месяца. Психологически развивалась нормально, и говорить начала рано, но это были не стандартные слова «мама», «папа», а «зайчик», «мишка» и др.
В 1 год и 7 мес. она перестала узнавать родителей и, казалось, не нуждалась в них. Весь день проводила за одним однообразным занятием: кидала мяч или катала коляску. Часами ходила по кругу, пока ее не останавливали или она запиналась. Такое стереотипное поведение носит название полевого, когда действие затягивает больного, и он не может ничего сделать.
В четыре года к симптомам присоединились эпилептоидные припадки. Однако по достижении школьного возраста девочка находилась на домашнем обучении, и делала некоторые успехи.
12–6 лет – это был период ремиссии, когда болезнь практически не беспокоила. Но с 16 лет появились новые, более глубокие проблемы, связанные с костными деформациями и болезнями внутренних органов. Одна нога девочки была короче другой почти на 10 см, что не могло не препятствовать ходьбе. В 20 лет она весила всего 24 кг с ростом 158 см.
Обычно СР протекает в 4 стадии.
Первая стадия, которая, как правило, стартует с 6 месяцев до полутора лет, проявляется нарастанием раздражительности и лабильностью настроения у ребенка. Эпизоды плача и психомоторного возбуждения сменяются все большей пассивностью. Малыш бесцельно передвигается по комнате, пропадает интерес к игрушкам. Но контакт с матерью сохраняется.
Вот как описывает женщина поведение своей дочери на заре заболевания: она кричала целый день без остановки, билась головой о стены, не могла уснуть. Что бы мы ни делали, она не успокаивалась. Это был настоящий ад. Но больше угнетало то, что ни один врач не мог поставить вразумительный диагноз.
Развивается диспропорция головы и конечностей по отношению к телу. Они становятся несоизмеримо маленькими. Замедляется рост, и снижается тонус мышц.
Вторая стадия, длящаяся несколько лет, отличается пестротой симптомов
Сразу обращает на себя внимание снижение интеллектуальных способностей, развивается умственное слабоумие. Происходит регресс практически всех полученных навыков
Речь полностью исчезает или переходит в степень эхолалии – механического повторения услышанного.
Приобретенные двигательные навыки, предметно-ролевое поведение теряются и замещаются двигательными стереотипами. Характерный симптом: многочисленно повторяющиеся движения, напоминающие мытье рук. Кроме этого, ребенок постоянно заламывает или потирает их, размахивает ими, хлопает в ладоши. Сжатие пальцев рук вполне нормально в 4 месяца, но в более позднем возрасте говорит об остановке развития. Малыш утрачивает хватательный рефлекс, не способен производить вращательные движения руками.
Постепенно двигательная активность сходит на нет. Нарушается походка, ребенок ходит, не сгибая коленей.
Третья стадия длится 10 лет и более, характеризуется она развитием стойкого, глубокого слабоумия, вплоть до идиотии. Наблюдается полная потеря способности говорить и понимать обращенную к ребенку речь. Появляется тремор всего тела, отягчающий движения. Усиливаются судорожные припадки.
Четвертая, конечная стадия – это период усугубления ранее проявляемых симптомов. Стойкая утрата умственных способностей, двигательных навыков, развитие мышечных дистрофий, приводящих к полному обездвиживанию.
Продолжительность жизни таких больных в среднем колеблется до 30 лет, хотя известны случаи, когда они доживали и до 50-летнего возраста.
Online-консультации врачей
| Консультация маммолога |
| Консультация специалиста в области лечения стволовыми клетками |
| Консультация невролога |
| Консультация диагноста (лабораторная, радиологическая, клиническая диагностика) |
| Консультация специалиста банка пуповинной крови |
| Консультация сосудистого хирурга |
| Консультация стоматолога |
| Консультация дерматолога |
| Консультация гастроэнтеролога |
| Консультация специалиста по лечению за рубежом |
| Консультация психоневролога |
| Консультация онколога-маммолога |
| Консультация уролога |
| Консультация сексолога |
| Консультация детского невролога |
Новости медицины
Футбольные фанаты находятся в смертельной опасности,
31.01.2020
«Умная перчатка» возвращает силу хвата жертвам травм и инсультов,
28.01.2020
Назван легкий способ укрепить здоровье,
20.01.2020
Топ-5 салонов массажа в Киеве по версии Покупон,
15.01.2020
Новости здравоохранения
Глава ВОЗ объявил пандемию COVID-19,
12.03.2020
Коронавирус атаковал уже более 100 стран, заразились почти 120 000 человек,
11.03.2020
Коронавирус атаковал 79 стран, число жертв приближается к 3200 человек,
04.03.2020
Новый коронавирус атаковал 48 стран мира, число жертв растет,
27.02.2020
1.Общие сведения
В современной неврологии одной из острых и актуальных проблем, для которой существуют пока лишь паллиативные решения, остается группа спинальных мышечных атрофий (СМА, SMA). Речь идет о наследственных заболеваниях, при которых из-за дефекта одного из генов изначально нарушен механизм питания т.н. моторных нейронов спинного мозга – нервных клеток, отвечающих за сократительную активность мускульных структур организма, – что приводит к постепенному их отмиранию.
К счастью, такая патология достаточно редка, однако среди наследственных заболеваний она является одной из наиболее часто встречаемых. Статистические данные по спинальной мышечной атрофии в различных источниках варьируют (примерно один случай на 6-8 тыс). Достоверно известно, что вероятность рождения больного ребенка при носительстве сбойного гена обоими родителями составляет 1/4 (25%); установлено также, что в случае «запуска» атрофического процесса с самого рождения шансы дожить до двухлетнего возраста не превышают 50%. Однако СМА может начаться в любом возрасте, обычно в интервале 20-50 лет.
Выделяют четыре типа спинальной мышечной атрофии. Синдром Кеннеди (спинобульбарная мышечная атрофия, СБМА) представляет собой взрослую смешанную форму, имеющую ряд отличительных особенностей. В частности, СБМА чаще встречается и протекает тяжелее у мужчин, чем у женщин; это связано с тем, что дефектный ген находится в Х-хромосоме.
Причины адреногенитального синдрома
В 90-95% случаев патология возникает при повреждении активного гена CYP21-B, который отвечает за синтез 21-гидроксилазы – фермента, влияющего на образование кортизола. В остальных клинических случаях АГС развивается вследствие дефектов ДНК, нарушающих производство других ферментов, обеспечивающих стероидогенез, – StAR/20,22-десмолазы, 3-β- гидрокси-стероиддегидрогеназы, 17-α-гидроксилазы/17,20-лиазы, 11-β-гидроксилазы, P450-оксидоредуктазы и синтетазы альдостерона.
Различают следующие виды адреногенитального синдрома:
-
сольтеряющий тип. Проявления болезни начинают обнаруживаться с первых недель жизни. У девочек половые органы формируются по мужскому типу, а у мальчиков увеличиваются пенис и мошонка. Из-за грубого нарушения образования стероидных гормонов развивается тяжелая рвота, понос, судороги, темнеет кожа. Прогрессирующее обезвоживание ведет к смерти при отсутствии своевременной заместительной терапии.
Через 2-3 дня от начала клинического проявления заболевания появляются симптомы дегидратации и развития метаболического ацидоза.
-
Простой вирильный. Преобладают нарушения развития половых органов. У девочек: увеличен клитор, похожий на половой член; углублен вход во влагалище; половые губы больше нормы; матка и придатки сформированы. У мальчиков: увеличен пенис, кожа мошонки имеет темную пигментацию. Девочки широкоплечие, с узким тазом, укороченными и массивными конечностями. У них низкий голос, кадык на шее, молочные железы не растут. У мальчиков рано появляются грубые волосы на подбородке и верхней губе, ломается голос.
С возрастом у пациентов нарастают признаки вирилизации вследствие стимулирующего действия андрогенов. Характерно ранее начало полового созревания в 3-5 лет.
-
Постпубертатный тип. Выявляют в молодом возрасте. Приобретенная форма возникает после появления опухоли в надпочечниках или при их повышенной активности.
Половые органы соответствуют полу, но развивается гипертрофия клитора и пениса. Основные нарушения встречаются у женщин – уменьшаются или прекращаются месячные (после стресса, травмы, аборта, выкидыша). Наступление первой менструации может быть только к 15 годам, цикл удлинен (более 30-40 дней). Кожа склонна к повышенной жирности и образованию угрей, имеется повышенное оволосение. При обследовании обнаруживают гиперплазию коркового слоя надпочечников.
Также имеются и варианты неклассического течения адреногенитального синдрома – с высоким давлением крови, с лихорадкой, липидный (ожирение, нарушение холестеринового обмена), с гирсутизмом (усиленный рост волос на теле и лице, по средней линии живота, около сосков).
Почему необходимо обратиться в клинику «Мама Папа Я»
Сеть семейных клиник «Мама Папа Я» расположена в Москве и других городах. При адреногенитальном синдроме оказываются такие медицинские услуги по доступной цене:
- лабораторная диагностика гормональных нарушений на современном оборудовании;
- прием профильных специалистов – педиатра, гинеколога, эндокринолога;
- последовательное наблюдение за ребенком, преемственность в лечении у докторов разного профиля;
- современные методы лечения при вынашивании беременности;
- назначение лекарственной терапии по современным методикам.
Врачи нашей клиники проводят раннюю диагностику и назначают грамотное лечение при любой форме заболевания. В таких условиях проявления адреногенитального синдрома хорошо корректируются. Записывайтесь на прием прямо сейчас!
Симптомы дисфункции коры надпочечников
При врожденном варианте адреногенитального синдрома фигура пациенток уже в детском возрасте приобретает мужские черты. У них рано закрываются зоны роста в костях, поэтому они имеют невысокий рост, грубеет голос, половые органы имеют неправильное строение (гипертрофированный клитор, видоизмененные половые губы напоминают мошонку).
Кроме классической формы АГС существуют :
- пубертатная, когда симптомы проявляются в переходном подростковом возрасте, в период физиологического усиления гормональной функции коры надпочечников;
- постпубертатная, когда проявления манифестируют в конце второго десятилетия жизни, часто после самопроизвольного выкидыша на раннем сроке беременности, неразвивающейся беременности или после медицинского аборта;
- латентная форма, единственным симптомом которой может быть невынашивание беременности на ранних сроках.
При исследовании кариотипа определяется 46 ХХ хромосом (женский набор). Внутренние половые органы также соответствуют женскому организму (матка, яичники). Половое созревание наступает рано (в 6-7 лет): оволосение развивается по мужскому типу, молочные железы слабо развиты, нередко отсутствуют менструации, однако, может присутствовать полноценный менструальный цикл. В дальнейшем пациенток с таким диагнозом ожидает бесплодие или привычное невынашивание плода.
Если же нарушение функции коры надпочечников вторично, пациентки жалуются на:
- внезапно появившееся избыточное оволосение (гирсутизм);
- нерегулярность менструального цикла;
- невозможность забеременеть;
- уменьшение молочных желез;
- увеличение размера клитора.
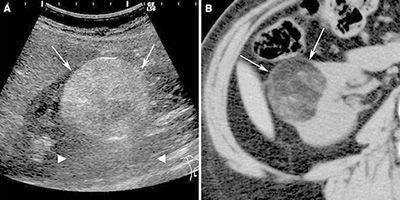
При выполнении УЗИ внутренних органов диагностируют недоразвитость или атрофию матки и яичников.
В обоих случаях патология может развиваться с преобладанием одного из синдромов:
- Сольтеряющий: пациентки отмечают общую вирилизацию (омужествление), гипотонию (сниженное артериальное давление), отеки.
- Гипертензивный: проявляется поражением миокарда и сосудов, повышением артериального давления.
- Вирилизация: фигура и голос пациенток становятся более мужскими, однако поражение внутренних органов отсутствует.
Виды урогенитальных расстройств
В XIX и начале XX вв. подобные проблемы были не актуальны, так как многие женщины просто не доживали до периода постменопаузы. В настоящее время урогенитальные расстройства наблюдаются у каждой третьей женщины, достигшей 55 лет и у семи женщин из десяти, достигших 70 лет.
Урогенитальный синдром (или урогенитальные расстройства, УГР) проявляется атрофическим вагинитом, уродинамическими и сексуальными нарушениями. Появление УГР напрямую связано с дефицитом эстрогенов, главных женских гормонов.
1
Урогенитальный синдром. Диагностика и лечение
2
Урогенитальный синдром. Диагностика и лечение
3
Урогенитальный синдром. Диагностика и лечение
Описание
Анализ полиморфизмов гена стероид-21-гидролаза (CYP21,10 точек) (адреногенитальный синдром) — генетическое исследование основных мутаций в генах стероид-21-гидролаза. Результаты анализа позволяют выявить причину развития патологии и назначить своевременное адекватное лечение.Адреногенитальный синдром — спектр заболеваний, обусловленных дефицитом ферментов, которые участвуют в синтезе стероидных гормонов в надпочечниках. Патология характеризуется повышенным уровнем андрогенов. Наиболее частая причина это дефицит 21-гидроксилазы. Заболевание передается по наследству, по аутосомно-рецессивному типу.
Ген фермента 21-гидроксилазы расположен на коротком плече хромосомы 6. Существует два гена — активный ген CYP21-B, кодирующий 21-гидроксилазу, и неактивный псевдоген CYP21-A. Эти гены в значительной мере гомологичны.
Различают следующие формы заболевания: вирильная, сольтеряющая, гипертензивная, вирильная с периодическими лихорадками. Симптомы заболевания могут развиться в любом возрасте.
Недостаток фермента в крови снижает содержание кортизола и альдостерона. Вследствие низкого уровня кортизола увеличивается секреция адренокортикотропного гормона, который способствует гиперплазии коры надпочечников, причём именно той её зоны, в которой синтезируются андрогены. Из-за этого концентрация андрогенов в крови повышается, и развивается адреногенитальный синдром.
Клинические проявления адреногенитального синдрома
Избыток андрогенов, начиная с ранних стадий развития плода, у новорождённых девочек обуславливает интерсексуальное строение наружных гениталий — женский псевдогермафродитизм. Выраженность изменений варьирует от простой гипертрофии клитора до полной маскулинизации гениталий: пенисообразный клитор с экстензией отверстия уретры на его головку.
Строение внутренних половых органов у плодов с женским генотипом при адреногенитальном синдроме всегда нормальное.
У мальчиков отмечаются увеличение размеров пениса и гиперпигментация мошонки.
У детей при отсутствии лечения в постнатальном периоде происходит быстрое прогрессирование вирилизации. Быстро закрываются зоны роста костей, в результате чего у взрослых больных, как правило, отмечается низкорослость.
У девочек при отсутствии лечения определяется первичная аменорея, связанная с подавлением гипофизарно-яичниковой системы избытком андрогенов. У взрослых женщин наблюдаются симптомы вирилизации: гипертрофия клитора, общий гипертрихоз, гирсутизм, атрофия молочных желёз, расстройство менструального цикла вплоть до аменореи. Нередко развивается бесплодие.
Надпочечниковая недостаточность развивается при сольтеряющих формах заболевания. Заболевание проявляется такими симптомами, как вялое сосание, рвота, обезвоживание, метаболический ацидоз, нарастающая адинамия. Развиваются характерные для надпочечниковой недостаточности электролитные изменения и дегидратация. Указанные симптомы в большинстве случаев манифестируют между 2-й и 3-й неделей после рождения ребенка. Одним из проявлений дефицита глюкокортикоидов является прогрессирующая гиперпигментация.Подготовка
Генетическое обследование не требует специальной подготовки.
Рекомендуется взятие крови не ранее чем через 4 часа после последнего приёма пищи.
Перед диагностикой не рекомендуется подвергать себя стрессовым ситуациям, принимать спиртные напитки и курить.
Рацион и приём лекарственных препаратов не влияет на результат исследования.Показания:
- неоднократные прерывания беременности на ранних сроках;
- внутриутробная гибель плода;
- неудачные попытки ЭКО;
- СПКЯ неустановленной этиологии;
- диагностика различных формы ВДКН у детей.
Интерпретация результатов
Для интерпретации результатов генетического тестирования требуется консультация врача-генетика.
Расстройство уродинамики
Из всех урогенитальных расстройств недержание мочи — одно из самых неприятных как в физическом, так и в психологическом смысле. Это отклонение негативно отражается на всех сферах жизнедеятельности, приводит к стрессу, ограничению подвижности, социальной изолированности. Частый спутник неудержания мочи — инфекции мочевыводящих путей.
Женщины с урогенитальными расстройствами чаще всего обращаются к урологу. Однако урогенитальный синдром, вызванный, в первую очередь, снижением выработки эстрогенов, должен лечить совсем другой специалист — гинеколог, тогда лечение достигнет нужного эффекта!
Различают стрессовое, ургентное и смешанное недержание мочи.
Стрессовое недержание мочи происходит при физической нагрузке (смех, кашель, изменение положения тела, поднятие тяжести), при резком повышении внутрибрюшного давления.
Ургентным недержанием мочи (УНМ) называется состояние, при котором больной испытывает частые внезапные позывы к мочеиспусканию.
При смешанном недержании происходит непроизвольная утечка мочи как в результате внезапного позыва на мочеиспускание, так и после кашля, чихания или какого-то физического движения.
Существуют также ночной энурез (мочеиспускание во время сна) и постоянное недержание мочи (когда подтекание мочи происходит все время).
Достаточно часто в медицинской литературе встречается понятие гиперактивного мочевого пузыря (ГМП). При этом состоянии отмечается учащенное мочеиспускание (свыше 8 раз в сутки, в том числе пробуждение в ночной период), непреднамеренная потеря мочи сразу после ургентного позыва к мочеиспусканию.
Нарушения мочеиспускания в той или иной мере знакомо многим женщинам зрелого возраста
Очень важно не оставаться один на один с проблемой, а обратиться к специалисту, который поможет найти максимально комфортное решение в данной ситуации. 1
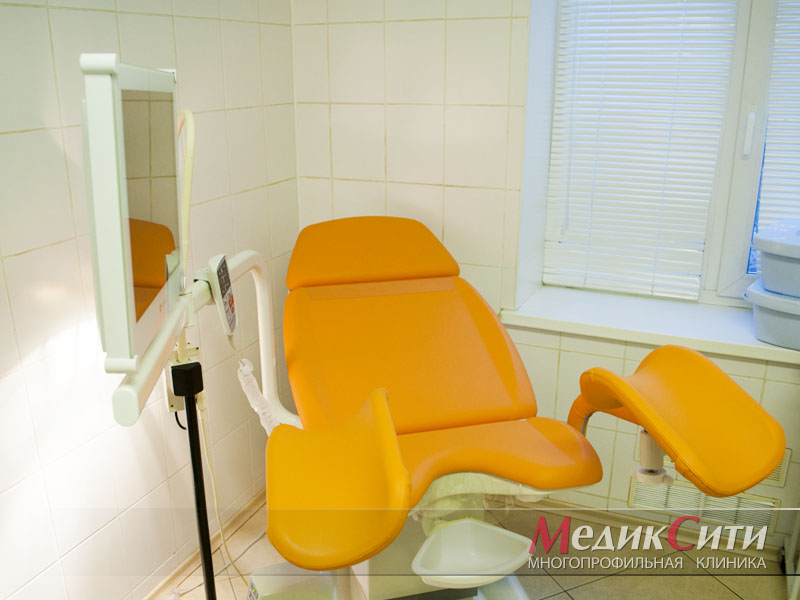
1
Кольпоскоп
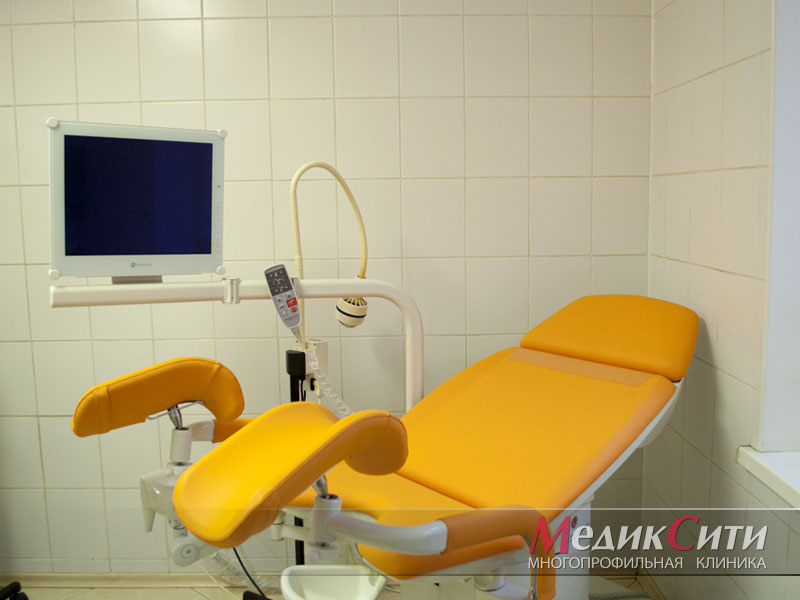
2
Кольпоскоп

3
Кольпоскоп
Диагностика заболевания заключается в следующем:
- сбор анамнеза (врач выслушивает жалобы больной о нарушениях, недержании мочи, выясняет, когда начались эти явления, сопровождаются ли они другими проявлениями урогенитальных расстройств);
- прокладочный тест (основан на измерении веса прокладки до физических упражнений и после часа занятий: увеличение веса прокладки более чем на 1 грамм может говорить о недержании мочи);
- бактериологическое исследование посева мочи и определение чувствительности к антибиотикам.
Уродинамическое обследование:
- урофлоуметрия — объективная оценка мочеиспускания, которая дает представление о скорости опорожнения мочевого пузыря;
- цистометрия — исследование емкости мочевого пузыря, давления в мочевом пузыре в момент его наполнения, при позыве к мочеиспусканию и во время мочеиспускания;
- профилометрия — метод диагностики, позволяющий изучить состояние аппарата, удерживающего мочу (наружный и внутренний сфинктеры мочеиспускательного канала).
К каким докторам следует обращаться если у Вас Дисфункция коры надпочечников (адреногенитальный синдром) и беременность:
Гинеколог
Нефролог
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Дисфункцим коры надпочечников (адреногенитального синдрома) и беременность, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору – клиника Eurolab всегда к Вашим услугам! Лучшие врачи осмотрят Вас, изучат внешние признаки и помогут определить болезнь по симптомам, проконсультируют Вас и окажут необходимую помощь и поставят диагноз. Вы также можете вызвать врача на дом. Клиника Eurolab открыта для Вас круглосуточно.
Как обратиться в клинику:
Телефон нашей клиники в Киеве: (+38 044) 206-20-00 (многоканальный). Секретарь клиники подберет Вам удобный день и час визита к врачу. Наши координаты и схема проезда указаны здесь. Посмотрите детальнее о всех услугах клиники на ее персональной странице.
Методы диагностики адреногенитального синдрома
Диагностика в период внутриутробного развития
При обследовании беременных о возможности гиперплазии надпочечников может свидетельствовать аномальное формирование половых органов плода. Это можно увидеть на втором скрининговом акушерском УЗИ. В таких случаях рекомендуется дополнительное обследование, назначается анализ амниотической жидкости или после 21 недели берут кровь плода (из пуповины под контролем УЗИ).
Диагностика после родов
После родов диагностика не представляет сложности. Назначается обследование: проба с АКТГ – нет повышения содержания кортизола после его введения; анализ крови – снижен натрий, повышен калий, 17 ОН-прогестерон в 5-7 раз и более, андростендион (предшественник стероидов), ренин (при сольтеряющей форме); анализ мочи – высокая концентрация 17-кетостероидов, после приема преднизолона снижается наполовину. В сомнительных случаях применяют кариотипирование для подтверждения женского кариотипа (46ХХ). Исследование мутаций в гене CYP11B1 – секвенирование на выявление мутации – His R448H.
Диагностика при позднем клиническом дебюте
Большее значение диагностический поиск приобретает при позднем клиническом дебюте или скрытом течении с минимальными внешними проявлениями вирилизации. В подобных ситуациях для выявления адреногенитального синдрома используют следующие лабораторные и инструментальные методы:
-
гормональный профиль (кортизол и предшественники, 17-ОНП, ДЭА-с и ДЭА, АКТГ и др.);
-
рентгенография костей кисти (раннее завершение роста);
-
УЗИ органов малого таза (признаки ановуляторного цикла), надпочечников (гиперплазии); в ряде случаев назначается МРТ, МСКТ исследование;
-
измерение базальной температуры. Температурная кривая типична для ановуляторного цикла: первая фаза растянута, вторая укорочена, что обусловлено недостаточностью желтого тела, которое не образуется из-за отсутствия овуляции).
Дифференциальная диагностика адреногенитальных расстройств, возникших в пубертатном и детородном возрасте, проводится с синдромом поликистозных яичников, овариальными андробластомами, андростеромами надпочечников, вирильным синдромом гипоталамического происхождения и конституциональным гирсутизмом. В сложных случаях к диагностике привлекают эндокринологов, урологов, врачей-генетиков.
Чтобы точно продиагностировать заболевание, запишитесь на прием к специалистам сети «Семейный доктор».
3.Симптомы и диагностика
Клиническая картина кардинальным образом зависит от того, в каком возрасте развивается синдром, является ли он врожденным или приобретенным. Типичными проявлениями считают увеличение размеров полового члена или клитора (в зависимости от пола), гиперпигментацию кожи, особенно на гениталиях, повышенную обволошенность, бесплодие, аменорею или олигоменорею, склонность к гипертонии (во многих источниках выделяется гипертоническая форма адреногенитального синдрома), невысокий рост с развитой по мужскому типу мускулатурой (у женщин) и относительно короткими конечностями.
Сольтеряющая форма опасна для жизни: дефицит альдостерона нарушает солевой метаболизм в почках, что может вызывать фонтанирующую рвоту независимо от приема пищи, нарушения сердечной деятельности и т.п. В дальнейшем сохраняется предрасположенность к геморрагическим инсультам, почечной недостаточности, офтальмопатологии и пр.
В наиболее выраженных случаях адреногенитального синдрома наблюдается гирсутизм, гермафродитизм и другие грубые аномалии развития.
Диагноз устанавливают на основании имеющей клиники, внешнего осмотра, инструментального исследования строения внутренних половых органов (УЗИ, при подозрении на опухоль надпочечников или сопутствующий поликистоз яичников – КТ, МРТ, рентгенография для исследования костных структур и т.д.). Обязательным является развернутый анализ крови на содержание гормонов и консультация медицинского генетика (а также других профильных специалистов в зависимости от конкретной формы и выраженности синдрома).
Механизм наследования генитального синдрома
При этом заболевании наблюдаются генетические аномалии, при которых нарушается выработка гормона надпочечников – кортизола.
Существует несколько вариантов болезни, при которых страдают различные гены, отвечающие за выработку белков, необходимых для образования гормонов. В большинстве случаев «ломается» ген CYP21, кодирующий 21-гидроксилазу. На такое нарушение приходится примерно 95% случаев болезни. Однако у некоторых детей имеется сбой выработки других шести ферментов, также участвующих в процессе образования кортизола.
Риск возникновения болезни зависит от особенностей наследственности:
- Если оба родителя являются носителями болезни, но сами не болеют, вероятность рождения ребенка с генитальным синдромом составляет 25%.
- В случае если один из родителей болен, а второй является носителем, риск появления на свет больных детей составляет 75%.
- У двоих родителей, страдающих адрено-генитальным синдромом, не обязательно все дети будут больны. Часть из них не заболеет, но станет носителями пораженного гена, который передастся потомству.
- В случае, если один из родителей здоров, а второй является носителем или болен генитальным синдромом, также возможно возникновение носительства измененных генов.
Самым эффективным методом предотвращения заболевания является сдача будущими родителями анализов на генетику. Это позволит выявить вероятность развития не только этого, но и других наследственных болезней.
Подготовка к анализу на генетику
При высоком риске заболевания можно прибегнуть к репродуктивным технологиям с применением предимплантационной диагностики. В этом случае зачатие происходит «в пробирке», а эмбрион подсаживают после обследования на генетические аномалии.
Патогенез (что происходит?) во время Адреногенитального синдрома:
Патогенетической сущностью адреногенитального синдрома является угнетение выработки одних кортикостероидов при одновременном увеличении выработки других вследствие дефицита того или иного фермента, обеспечивающего один из этапов стероидогенеза. В результате дефицита Р450с21 нарушается процесс перехода 17-гидроксипрогестерона в 11-дезоксикортизол и прогестерона в дезоксикортикостерон.
Таким образом, в зависимости от выраженности дефицита фермента развивается дефицит кортизола и альдостерона. Дефицит кортизола стимулирует продукцию АКТГ, воздействие которого на кору надпочечника приводит к ее гиперплазии и стимуляции синтеза кортикостероидов, — стероидогенез смещается в сторону синтеза избытка андрогенов. Развивается гиперандрогения надпочечникового генеза. Клинический фенотип определяется степенью активности мутировавшего гена CYP21-B. При ее полной утрате развивается сольтеряющий вариант синдрома, при котором нарушается синтез глюкокортикоидов и минералокортикоидов. При сохранена умеренной активности фермента минералокортикоидная недостаточность не развивается в связи с тем, что физиологическая потребность в альдостероне примерно в 200 раз ниже, чем в кортизоле. Выделяют 3 варианта дефицита 21-гидроксилазы:
- дефицит 21-гидроксилазы с сольтеряющим синдромом;
- простая вирильная форма (неполный дефицит 21-гидроксилазы);
- неклассическая форма (постпубертатная).
Распространенность адреногенитального синдрома значительно варьирует среди разных национальностей. Среди представителей европейской расы распространенность классических вариантов (сольтеряюший и простой) дефицита 21-гидроксилазы составляет примерно 1 на 14000 новорожденных. Значительно выше этот показатель у евреев (неклассическая форма дефицита 21-гидроксилазы — до 19 % евреев Ашкенази). Среди эскимосов Аляски распространенность классических форм дефицита 21-гидроксилазы составляет 1 на 282 новорожденных.