Костный мозг где находится? костный мозг: функции, строение
Содержание:
Стоимость пересадки костного мозга
Стоимость хирургического вмешательства варьируется в весьма высоких диапазонах. Ведь найти донора и провести саму процедуру не так просто. Во многих случаях это занимает длительное время. Ситуации бывают разные. Поэтому порой приходится не только долго ждать донора, но еще и проводить массу мероприятий перед самой операцией.
Стоимость полностью зависит от сложности операции. Естественно, в общую сумму входит и квалификация клиники и профессионализм врачей. Многое зависит и от страны, где проводится сама операция. Так, в Москве такая процедура может, стоить от 650 тыс. рублей до 3-х миллионов. В Санкт-Петербурге цена колеблется в район 2-х миллионов рублей.
Что касается дальнего зарубежья, то в Германии операция стоит 100 000 – 210 000 тыс. евро. Все зависит от самой работы и сложно процедуры. В Израиле стоимость хирургического вмешательства при родственном доноре колеблется в районе 170 тыс. долларов, при не родственном достигает 240 тыс. долларов.
[], [], [], [], [], [], []
Сколько стоит пересадка костного мозга?
Следует, сразу же оговорится, что процедура дорогостоящая. На цену влияет многое. Так, первым делом это специализация клиник и место ее расположения. Потому как израильские и немецкие медицинские центры являются самыми дорогими. Здесь стоимость операции варьируется в районе 200 000 тыс. евро. Но, несмотря на это, клиники действительно лучшие в своем роде.
На цену влияет и профессионализм врача, но это отражается минимально. Многое зависит от сложности самой процедуры. Так, стоимость зависит от родственности донора. В России операция будет, стоит около 3-х миллионов рублей. Кроме того, даже консультации перед процедурой платные.
Но когда речь идет о спасении жизни человека, цена особой роли не играет. Она не является выдуманной. Стоимость операции обусловлена ее сложностью.
Васкуляризация. Иннервация. Возрастные изменения. Регенерация.
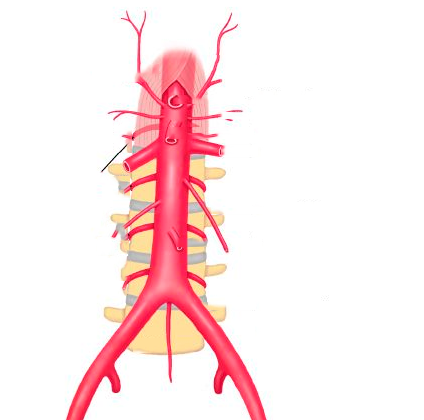
Васкуляризация. Костный мозг снабжается кровью посредством сосудов, проникающих через надкостницу в специальные отверстия в компактном веществе кости. Войдя в костный мозг, артерии разветвляются на восходящую и нисходящую ветви, от которых радиально отходят артериолы. Сначала они переходят в узкие капилляры (2—4 мкм), а затем в области эндоста продолжаются в широкие тонкостенные с щелевидными порами синусы (диаметром 10—14 мкм). Из синусов кровь собирается в центральную венулу. Постоянное зияние синусов и наличие щелей в эндотелиальном пласте обусловливаются тем, что в синусах гидростатическое давление несколько повышено, так как диаметр выносящей вены меньше по сравнению с диаметром артерии. К базальной мембране с наружной стороны прилежат адвентициальные клетки, которые, однако, не образуют сплошного слоя, что создает благоприятные условия для миграции клеток костного мозга в кровь. Меньшая часть крови проходит со стороны периоста в каналы остеонов, а затем в эндост и синус. По мере контакта с костной тканью кровь обогащается минеральными солями и регуляторами кроветворения.
Кровеносные сосуды составляют половину (50%) массы костного мозга, из них 30% приходится на синусы. В костном мозге разных костей человека артерии имеют толстую среднюю и адвентициальную оболочки, многочисленные тонкостенные вены, причем артерии и вены редко идут вместе, чаще врозь.
Капилляры бывают двух типов: узкие 6—20 мкм и широкие синусоидные (или синусы) диаметром 200—500 мкм. Узкие капилляры выполняют трофическую функцию, широкие являются местом дозревания эритроцитов и выхода в кровоток разных клеток крови. Капилляры выстланы эндотелиоцитами, лежащими на прерывистой базальной мембране.
Иннервация. В иннервации участвуют нервы сосудистых сплетений, нервы мышц и специальные нервные проводники к костному мозгу. Нервы проникают в костный мозг вместе с кровеносными сосудами через костные каналы. Далее покидают их и продолжаются как самостоятельные веточки в паренхиме в пределах ячеек губчатого вещества кости. Они ветвятся на тонкие волоконца, которые либо вновь вступают в контакт с костномозговыми сосудами и оканчиваются на их стенках, либо заканчиваются свободно среди клеток костного мозга.
Возрастные изменения. Красный костный мозг в детском возрасте заполняет эпифизы и диафизы трубчатых костей и находится в губчатом веществе плоских костей. Примерно в 12—18 лет красный костный мозг в диафизах замещается желтым. В старческом возрасте костный мозг (желтый и красный) приобретает слизистую консистенцию и тогда называется желатинозным костным мозгом. Следует отметить, что этот вид костного мозга может встречаться и в более раннем возрасте, например при развитии костей черепа и лица.
Регенерация. Красный костный мозг обладает высокой физиологической и репаративной регенерационной способностью. Источником образования гемопоэтических клеток являются стволовые клетки, находящиеся в тесном взаимодействии с ретикулярной стромальной тканью. Скорость регенерации костного мозга в значительной мере связана с микроокружением и специальными ростстимулирующими факторами гемопоэза.
Некоторые термины из практической медицины:
- миелограмма (миело- + греч. gramma запись) — выраженный в форме таблицы или диаграммы результат микроскопии мазка пунктата костного мозга, отражающий качественный и количественный состав ядросодержащих клеток миелоидной ткани.;
- миелоидная реакция (миело- + греч. —eides подобный) — появление в периферической крови малодифференцированных клеток, относящихся к грануло- и эритропоэтическому ряду; наблюдается при метастазах злокачественной опухоли в костный мозг, а также при сепсисе, туберкулезе и некоторых других болезнях;
- остеомиелит (osteomyelitis; остео- + греч. myelos костный мозг + ит; син.: костоеда — устар., паностит) — воспаление костного мозга, обычно распространяющееся на компактное и губчатое вещество кости и надкостницу;
| Часть первая – Общая характеристика, классификация; красный костный мозг | immunesys1.mp37 122 кБ |
| Часть вторая – Вилочковая железа — тимус | immunesys2.mp35 310 кБ |
| Часть третья – Селезенка | immunesys3.mp36 073 кБ |
| Часть четвертая – Лимфатические узлы, лимфоидная ткань слизистых оболочек | immunesys4.mp37 152 кБ |
Структура и виды костного мозга
Орган состоит из стромы и кроветворных элементов. Между ними есть определенная взаимосвязь. Зачатки гемопоэза формируются из зон эритроцитов, лейкоцитов и тромбоцитов. Стволовые клетки производят форменные элементы. Вне костномозговой ткани встречаются созревшие формы. Процесс контролируется гемопоэтическими соединениями. Орган является центральным и полипотентным периферическим лимфоидным органом тела человека. Выделяют такие разновидности: красную и желтую ткани. Рассмотрим функции красного костного мозга и функции желтого костного мозга.
Красный мозг
Так называемая красная костная ткань или ККМ находиться внутри трубчатых костей (диафизе), а так же в плоских костях и позвонках. Она представлена стромой и ретикулярной тканью. Орган считают фабрикой, которая образовывает из стволовых клеток другие элементы крови. Он принимает участие в иммунопоэзе – обмене питательных ценностей (белки, жиры, углеводы, минералы), костеобразовании.
ККМ проводит клетки крови по линиям гемопоэза. Его основная функция – это кроветворение (образование, созревание, вымывание элементов крови). Стоит отметить, что название клеток – колониеобразующие элементы(КОЭ) или колониеобразующие единицы (КОЕ). Еще в состав красного мозга входят три компонента – гемопоэтический, сосудистый и стромальный.
Желтый костный мозг
Желтая костная ткань или ЖКМ находится рядом с красной. Она выполняет резервную функцию, то есть, при сильном кровотечении данное вещество заполняет гемопоэтическими клетками место разрыва. Это помогает быстро восстановить свойства крови. В ее составе содержится большое скопление жировой ткани. Масса ЖКМ составляет около половины массы всей ткани.
Все остальное – ККМ. Основа органа – это рыхлая ретикулярная соединительная ткань. В ней присутствует скопление клеток. Желтая костная ткань заполняет пустые полости костей. Она считается резервом для ККМ. При кровопотерях создаются гемопоэтические элементы, которые помогают воссоздать ККМ. В ЖКМ есть участки миелоидной ткани, которые свойственные красному.
Симптомы
Основные клинические проявления миелодиспластического синдрома неспецифические и являются следствием изменения количества клеток крови. В первую очередь это цитопенический синдром, то есть совокупность состояний, вызванных снижением количества определённых клеток в периферической крови. Могут быть отдельно выделены следующие синдромы:
- анемический синдром — возникает при снижении количества эритроцитов и\или гемоглобина. Включает в себя бледность кожных покровов и видимых слизистых оболочек, слабость, повышенную утомляемость, раздражительность, шум или звон в ушах, головокружение, одышку, возникновение сердцебиения даже при незначительной физической нагрузке, выпадение волос, изменения ногтей (исчерченность ногтевых пластинок, принятие ими ложкообразной формы). Также могут возникать заеды в углах рта, глоссит (налёт, чувство жжения в языке, потеря вкусовой чувствительности), извращение вкуса и запаха, в ряде случаев дизурические расстройства. Встречается у подавляющего количества больных.
- геморрагический синдром — возникает в результате снижения количества тромбоцитов. Проявляется повышенной кровоточивостью — появлением кровоизлияний в кожу и слизистые оболочки размерами от синячков до крупных гематом, кровотечений (носовых, маточных, из дёсен, желудочно-кишечных кровотечений) и кровоизлияний во внутренние органы (головной мозг, сетчатка, суставы).
- лейкопения — снижение количества лейкоцитов. Поскольку лейкоциты являются основным звеном клеточного иммунитета, то присоединяются инфекции, которые и обуславливают дальнейшую симптоматику. Довольно часто, примерно в половине случаев, встречается только изолированная нейтропения — снижение количества только одного вида лейкоцитов, нейтрофилов. Кроме того, наблюдается постепенное ослабление организма, повышение температуры, озноб, учащённый пульс, беспокойство, головные боли.
К иным симптомам относят:
- инфекционные осложнения,
- В-симптомы (лихорадка, ночные поты, потеря веса),
- Увеличение селезёнки,
- аутоиммунные проявления. В 10% случаев являются самыми первыми проявлениями миелодиспластического синдрома: возникает системный васкулит, некротический панникулит, серонегативный артрит, ревматическая полимиалгия, Кумбс-положительная гемолитическая анемия, перикардит, плеврит.
При этом нельзя не отметить, что у значительного количества больных относительно доброкачественными формами миелодиспластического синдрома долгое время может не проявляться вообще никаких симптомов, и в этом случае заболевание может быть случайной находкой, выявленной впервые при выполнении общего анализа крови.
Популярные вопросы
Может ли остеома привести к раку?
Нет. Остеома – доброкачественная опухоль. Она может вызывать неблагоприятные для здоровья последствия для здоровья, если прорастает в полость черепа. Но вероятность перерождения в рак близка к нулю.
Что вызывает появление остеомы?
Причины появления опухоли неизвестны. Установлена роль наследственной предрасположенности. Если у ваших родственников диагностирована остеома, у вас она появится с большей вероятностью, чем в среднем в популяции. Пусковым фактором роста остеомы может быть травма кости или острый воспалительный процесс. Существует также теория пороков внутриутробного развития. Поводом для её возникновения стал тот факт, что остеома чаще всего развивается на стыке лобной и решётчатой кости, где развиваются мембранные и хрящевые ткани во время эмбриогенеза.
Нужно ли удалять остеому?
Опухоль растёт очень медленно. В большинстве случаев она не опасна. Удаляют только клинически значимые остеомы, которые могут прорасти в орбиту или кости черепа. Операция также может проводиться по эстетическим показаниям.
- Кудайбергенова С.Ф. Остеома носовой полости / С.Ф. Кудайбергенова // Вестник КАЗНМУ. — 2012. — № 2. — С. 92-93.
- Торопова И.А. Особенности клинического течения остеомы носа и околоносовых пазух / И.А. Торопова // Вестник РУДН. — Серия Медицина. — 2005. — № 1(29). — С. 95-97.
Цитологическое и гистологическое исследование
Мазки костного мозга готовят сразу после взятия пункции. Биоптат для гистологического исследования консервируют в специальных растворах. В лаборатории из биоптата готовят гистологические срезы, окрашивают их и оценивают. При этом стараются приготовить как можно больше микропрепаратов КМ, особенно при гипопластических процессах, когда взятые образцы очень бедны клеточными элементами. Цитологическое исследование проводится в день отбора образцов, на гистологию требуется до 10 дней.
При цитологическом исследовании миелограммы оценивают:
- количество и соотношение разных видов клеток;
- патологические изменения формы, размеров и структуры клеточных элементов;
- тип кроветворения;
- цитоз;
- костномозговые индексы;
- наличие специфических клеток.
Результат цитологического исследования имеет вид таблицы из трех колонок: в первой указаны названия клеточных элементов, во второй — показатели, определенные в образцах КМ, в третьей — референсные (нормальные) количественные или процентные показатели.
Что такое костный мозг
Костный мозг для кроветворной системы является важнейшим органом, ведь его главная функция – как раз осуществление гемопоэза, или кроветворения. Он непосредственно участвует в создании новых клеток крови взамен тех, что погибли, отмерли. Кроме того, единственной тканью взрослого человека, в которой содержатся незрелые клетки, известные также как стволовые, является именно костный мозг.
Костный мозг бывает двух типов: желтый, который представлен преимущественно жиром, и красный – основной орган кроветворения. В отличие от красного, желтый костный мозг не принимает участия в гемопоэзе.
Во время гемопоэза образуются клетки крови. Стартует гемопоэз в раннем эмбриональном периоде. Соответственно, существуют как эмбриональные кроветворные органы, так и те, что функционируют после рождения. К органам, которые отвечают за гемопоэз во время эмбрионального периода, относят желточный мешок, фетальную печень, селезенку и костный мозг. В желточном мешке появляются первые кроветворные стволовые клетки. Происходит это на 3-й неделе эмбриогенеза. Незадолго после, от 3-го месяца и до рождения, основным кроветворным органом плода становится печень, поскольку некоторые из стволовых клеток перемещаются туда. С 4-го же месяца эмбриогенеза начинается формирование клеток крови и в костном мозге. Кроме того, в кроветворении у плода участвуют тимус, лимфатические узлы и селезенка. В печени и селезенке сохраняются гемопоэтические стволовые клетки, находящиеся в «спящем» состоянии, чем часто объясняют факт возникновения за пределами костного мозга очагов кроветворения. Такое кроветворение называется экстрамедуллярным. Возникает оно при онкологических заболеваниях крови и в результате чрезмерной стимуляции гемопоэза.
Объем костномозговых полостей у только что родившегося ребенка составляет около 1,6 л., из которых красный костный мозг занимает почти 100% пространства. Когда человек взрослеет, происходит централизация кроветворения, при этом гемопоэтически активная ткань сохраняется в костях центральной части скелета. Общий объем костного мозга у взрослых достигает приблизительно 4 л.
Расположение гемопоэтической ткани у взрослого человека следующее: в костях таза ее больше всего – 40%, в телах позвонков значительно меньше – 28%, в костях черепа она составляет 13%, в эпифизах трубчатых костей и ребрах – 8%, в грудине меньше всего – только 2%. Оставшуюся часть костномозговых полостей занимает желтый костный мозг, являющийся, как вы помните, жировой тканью. При этом красный и желтый костный мозг находятся в равном соотношении: 1:1.
Структурно красный костный мозг подразделяется на: экстраваскулярный (собственно, гемопоэтическая ткань) и васкулярный, который состоит из широких венозных сосудов, называемых синусами. В сети ретикулиновых волокон внутри костных трабекул находится желеподобный дисперсный материал, который и является гемопоэтической тканью.
Кровоснабжение костного мозга называется перфузией. Его осуществляют основная питающая артерия и ее малые терминальные артериолы. Отток же крови происходит таким образом: по венозным капиллярам собирается кровь в центральный венозный синус через венозные сосуды. Стенки венозных сосудов состоят из следующих трех слоев клеток: адвентиции, базальной мембраны и эндотелия. Именно в ретикулуме – тонкой сети волокон соединительной ткани, образованной отростками адвентициальных клеток, располагаются кроветворные клетки. На объем гемопоэтического пространства влияют изменения в адвентициальных клетках: количество кроветворных клеток снижается, когда адвентициальные клетки увеличиваются из-за повышения содержания в них жира. Если рассматривать эту картину под микроскопом, она выглядит как трансформация красного костного мозга в желтый.
В тот момент, когда требования к кроветворению повышаются – адвентициальные клетки уменьшаются, тем самым способствуя увеличению гемопоэтического компонента костного мозга.
4.Приживление костного мозга
До того момента, когда пересаженные стволовые клетки приживутся в новом для них организме и начнут работать, производя кровь и возвращая утраченный иммунитет, проходит 2-4 недели. В течение всего этого периода главной задачей является, в буквальном смысле слова, сохранение жизни больному. Высокие дозы химиотерапии перед трансплантацией полностью уничтожают иммунитет, состав крови почти не позволяет организму самостоятельно бороться с инфекциями и предотвращать кровотечения. На поддержание жизнедеятельности направлен ряд регулярных процедур: переливания крови, профилактический приём антибиотиков, постоянный ввод препаратов, снижающие риск отторжения нового костного мозга.
Принимаются также чрезвычайные асептические меры, по возможности исключающие занесение в палату вирусов и бактерий. Строго ограничиваются посещения, предметы и еда, которые передаются больному. Сам больной при необходимости выйти из палаты надевает перчатки, халат и маску, чтобы уменьшить риск инфицирования в нестерильной среде. Воздух в палате подвергается постоянной фильтрации и очистке.
Ежедневно у больного проводится забор анализов крови, позволяющий контролировать процессы приживления костного мозга и динамику выработки кровяных телец. По мере того, как новые стволовые клетки начинают выполнять свои функции, постепенно отменяются реабилитационные процедуры и снижается уровень изоляции от окружающей среды.
Весь период реабилитации длится от 4 до 8 недель. Большую часть времени состояние пациента остаётся достаточно тяжёлым: тошнота, выраженная слабость, поносы, лихорадка, изъязвление слизистых, кровотечения. Самочувствие схоже с симптоматикой гриппа, только очень затяжного, что само по себе истощает и без того ослабленный организм. Состояние изо дня в день может колебаться от удовлетворительного до очень тяжёлого. При всех болезненных и опасных проявлениях оказывается срочная симптоматическая медицинская помощь.
Когда анализы показывают, что приживление костного мозга прошло успешно и больной больше не нуждается в поддерживающих и реабилитационных процедурах, врач принимает решение о выписке пациента. Как правило, ещё в течение года с этого момента человек не может вернуться в состояние полной работоспособности. Он очень слаб и должен регулярно посещать больницу для контроля состава крови, получения некоторых препаратов и даже переливаний крови, поскольку в этот период уровень необходимых кровяных телец может сильно снижаться. Не рекомендуется посещение мест большого скопления людей, полноценная активная жизнь и привычная деятельность не представляются возможными до тех пор, пока не произойдёт полное восстановление сил и не будет достигнута стабильность в работе нового костного мозга.
Противопоказания к пересадке костного мозга
Противопоказания, в первую очередь, создают острые инфекционные заболевания, такие, как ВИЧ, гепатит В и гепатит С, сифилис, всевозможные нарушения иммунной системы, а также беременность. Не рекомендуется операция по замене стволовых клеток слабым физически и пожилым пациентам, а также строго противопоказана пациентам, страдающим тяжелыми заболеваниями внутренних органов. Противопоказания могут также создавать долговременная терапия с применением антибиотиков или гормональных препаратов.
Противопоказаниями к донорству стволовых клеток, является заболевание донора аутоиммунным или же инфекционным заболеванием. Наличие любого из заболеваний легко выясняется путем обязательного медицинского всестороннего обследования донора.
Но, сегодня по-прежнему самым серьезным препятствием при процедуре замены стволовых клеток, остается несовместимость донора и пациента. Очень маленький шанс найти подходящего и совместимого донора для трансплантации. Зачастую донорский материал берется либо у самого пациента, либо у его физиологически совместимых родственников.
Прогноз
В силу развития цитопенических синдромов, особенно при снижении количества тромбоцитов, само по себе заболевание может быть жизнеугрожающим, но главная опасность миелодиспластического синдрома — перерождение его в острый лейкоз. Для оценки общей продолжительности жизни и риска трансформации миелодиспластического синрома в лейкоз используются две шкалы — International Prognostic Scoring System (IPSS) и шкала ВОЗ. В обеих шкалах используется балльная система, оценивающая кариотип, наличие цитопении (в шкале IPSS) или выраженной анемии (в шкале ВОЗ), а также количество бластов в костном мозге (шкала IPSS) или изначальный вариант миелодиспластического синдрома (шкала ВОЗ). Согласно сумме баллов и оценивается прогноз, а также планируется терапия и динамическое наблюдение.
Миелодиспластический синдром объединяет в себе несколько заболеваний, различных по степени тяжести и по их течению; кроме того, в рамках одного заболевания возможны различные проявления его с различной степенью тяжести. К сожалению, миелодиспластический синдром на данный момент является практически неизлечимым заболеванием, но своевременное обращение к врачу, грамотно подобранная терапия и тщательное динамическое наблюдение способны предотвратить злокачественное перерождение и контролировать его течение, сохраняя пациенту долгую жизнь с минимальным нарушением её качества.
Запись на консультацию круглосуточно
+7 (495) 151-14-53+7 (861) 238-70-54+7 (812) 604-77-928 800 100 14 98
Список литературы:
- Миелодиспластический синдром. Клинические рекомендации Ассоциации Онкологов России, 2019.
- Миелодиспластический синдром у взрослых. Клинические рекомендации Национального гематологического общества, 2014.
- Усс А.Л. Миелодиспластический синдром: классификация, прогноз, лечение. Проблемы здоровья и экологии. С.57-62.
- Косанова А.К. и соавт. Рефрактерные анемии и цитопении как диагностические критерии при миелодиспластических синдромах. Вестник КазНМУ, 2015, № 1. С. 131-133.
- Кохно А.В. и соавт. Миелодиспластический синдром. Клиническая геронтология. 2009. № 3. С. 33-46.
- Зельцер А.Н. Миелодиспластический синдром: трудности и успехи диагностики. Журнал фундаментальной медицины и биологии. 2017. № 1. С. 27-37.
- Myelodysplastic Syndromes. NCCN Guideline version 2.2020.